ความแตกต่างที่สำคัญ: อะตอมเป็นหน่วยพื้นฐานที่สสารทั้งหมดสร้างขึ้น อะตอมมีขนาดเล็กตั้งแต่ 0.1 ถึง 0.5 นาโนเมตรในความกว้าง แต่ละอะตอมขององค์ประกอบใด ๆ ประกอบด้วยโปรตอนนิวตรอนและอิเล็กตรอน อะตอมของธาตุต่าง ๆ มารวมตัวกันเพื่อสร้างโมเลกุล สิ่งนี้เกิดขึ้นผ่านปฏิกิริยาทางเคมี โมเลกุลเป็นสารเคมีที่มีอยู่น้อยที่สุด
องค์ประกอบคือสารเคมีบริสุทธิ์ที่มีอะตอมหนึ่งหรือหนึ่งชนิดซึ่งแตกต่างกันตามเลขอะตอม เลขอะตอมนั้นได้มาจากจำนวนของโปรตอนที่มีอยู่ในนิวเคลียสของธาตุ มีองค์ประกอบทั้งหมด 118 รายการที่ได้รับการจำแนกแบ่งระหว่างโลหะเมทัลรอยด์และอโลหะ แต่ละองค์ประกอบมีชุดคุณสมบัติของตนเอง องค์ประกอบส่วนใหญ่มีอยู่บนโลกในขณะที่บางส่วนได้รับการพัฒนาโดยใช้ปฏิกิริยานิวเคลียร์ องค์ประกอบอยู่ในรูปแบบ rawest แล้วและไม่สามารถแยกย่อยได้อีก องค์ประกอบทั้งหมดสามารถพบได้ในตารางธาตุซึ่งแสดงรายการตามเลขอะตอม
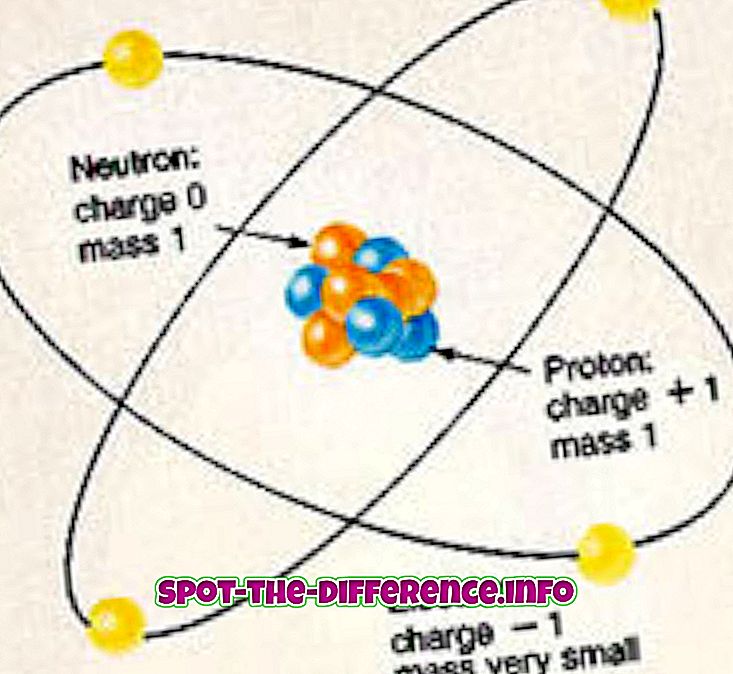
แต่ละอะตอมขององค์ประกอบใด ๆ ประกอบด้วยโปรตอนนิวตรอนและอิเล็กตรอน โปรตอนและนิวตรอนประกอบด้วยนิวเคลียสของอะตอมและตั้งอยู่ตรงกลางของอะตอม นิวเคลียสถูกล้อมรอบด้วยกลุ่มเมฆของอิเล็กตรอนซึ่งถูกผูกไว้กับนิวเคลียสด้วยแรงแม่เหล็กไฟฟ้า อิเล็กตรอนมีประจุลบซึ่งเป็นวิธีดึงดูดนิวเคลียสเนื่องจากโปรตอนในนิวเคลียสมีประจุเป็นบวก ในทางกลับกันนิวตรอนไม่มีประจุ
จำนวนโปรตอนนิวตรอนและอิเล็กตรอนในอะตอมเป็นตัวกำหนดว่ามันคือองค์ประกอบใด ตัวอย่างเช่นอะตอมของเหล็กมี 26 โปรตอน 30 นิวตรอนและ 26 อิเล็กตรอน อะตอมเหล็กแต่ละตัวจะมีการกำหนดค่านี้
อะตอมของธาตุต่าง ๆ มารวมตัวกันเพื่อสร้างโมเลกุล สิ่งนี้เกิดขึ้นผ่านปฏิกิริยาทางเคมี ตัวอย่างเช่นอะตอมไฮโดรเจนสองอะตอมและออกซิเจนหนึ่งอะตอมรวมกันเพื่อสร้างโมเลกุลของน้ำ

โมเลกุลสามารถมีคุณสมบัติแตกต่างกันมากจากองค์ประกอบที่ทำจาก ตัวอย่างเช่น: น้ำมีพฤติกรรมแตกต่างจากออกซิเจนหรือไฮโดรเจนอย่างมากแม้ว่าจะประกอบด้วยอะตอมไฮโดรเจนสองอะตอมและออกซิเจนหนึ่งอะตอม
นอกจากนี้อะตอมไม่สามารถดำรงอยู่ได้อย่างเป็นอิสระในธรรมชาติโดยไม่ต้องผูกมัดกับบางสิ่ง เราจะไม่พบเพียงอะตอมออกซิเจนเดียวหรืออะตอมคาร์บอนเดียว มันมักจะถูกผูกมัดกับบางสิ่งบางอย่างเช่น O2 (ออกซิเจน) หรือ CO2 (คาร์บอนไดออกไซด์) เมื่อถูกผูกเข้ากับโมเลกุลโมเลกุลนั้นสามารถดำรงอยู่ได้โดยอิสระในธรรมชาติซึ่งเป็นสาเหตุที่ทำให้เราสามารถค้นหาโมเลกุลของออกซิเจนโมเลกุลของคาร์บอนไดออกไซด์โมเลกุลของน้ำ (H2O) เป็นต้น
ในโมเลกุลอะตอมจะติดกันในรูปแบบหรือรูปแบบเฉพาะ นี่ขึ้นอยู่กับจำนวนพันธะที่อะตอมสามารถทำได้ อะตอมก่อตัวเป็นโมเลกุลโดยสร้างพันธะเคมีขึ้นมา อะตอมของออกซิเจนจะมีพันธะสองพันธะกับอะตอมอื่น ๆ อะตอมของคาร์บอนจะมีพันธะสี่พันธะกับอะตอมอื่นและอะตอมของไนโตรเจนจะมีพันธะสามกับอะตอมอื่นเสมอ ด้วยเหตุนี้โมเลกุลบางชนิดจึงมีรูปร่างเฉพาะเสมอเช่นห้าเหลี่ยมหกเหลี่ยมหกเหลี่ยมด้านข้างสองข้าง ฯลฯ
โมเลกุลมักจะรวมตัวกันเป็นกลุ่มการก่อตัวขึ้นอยู่กับสถานะของพวกเขา เช่นในสถานะก๊าซโมเลกุลมีแนวโน้มที่จะบินไปรอบ ๆ ในสถานะของเหลวโมเลกุลมีแนวโน้มที่จะรวมตัวกันอย่างหลวม ๆ เพื่อให้พวกเขายังคงเคลื่อนไหวได้ ในขณะที่อยู่ในสถานะของแข็งโมเลกุลจะถูกอัดแน่นเข้าด้วยกันและสามารถสั่นสะเทือนได้เท่านั้น
โมเลกุลมักจะแสดงในสูตรโมเลกุล ตัวอย่างเช่น: O2, H2O, CO2, C6H12O6 (น้ำตาล) สูตรโมเลกุลคือชื่อขององค์ประกอบตามด้วยจำนวนอะตอมขององค์ประกอบนั้นในโมเลกุล