Key Difference: Molarity ยังเป็นที่รู้จักกันในนามความเข้มข้นของฟันกรามวัดจำนวนโมลของสารที่มีอยู่ในลิตรต่อการแก้ปัญหา โมลาริตีแสดงด้วยเมืองหลวง M. Molality วัดจำนวนโมลของสารที่มีอยู่ในตัวทำละลายต่อกิโลกรัม Molality แสดงด้วยตัวพิมพ์เล็ก m
แนวคิดทั้งสองนี้จะคำนวณตามจำนวนโมลที่มีอยู่ในโซลูชันปัจจุบัน วิธีการแก้ปัญหาสามารถกำหนดเป็นส่วนผสมที่เป็นเนื้อเดียวกันซึ่งหมายความว่าสองคนหรือมากกว่าส่วนประกอบได้รับการผสมจนถึงจุดที่มันไม่สามารถแยกแยะได้ด้วยตาเปล่า แนวคิดทั้งสองนี้ต้องการโมลการทำความเข้าใจเนื่องจากมันเป็นตัวกำหนดจำนวนโมลที่มีอยู่ในการแก้ปัญหา ทฤษฎีของโมลถูกค้นพบโดยนักวิทยาศาสตร์ชาวอิตาลี Amedeo Avogardo
ในปี 1811 อโวการ์โดเสนอว่าปริมาณของก๊าซที่อุณหภูมิและความดันที่กำหนดนั้นเป็นสัดส่วนกับจำนวนของอะตอมหรือโมเลกุลโดยไม่คำนึงถึงลักษณะของมัน แนวคิดนี้เรียกว่าค่าคงที่ Avogardo มันถูกกำหนดให้เป็นจำนวนของอนุภาคที่เป็นองค์ประกอบ (ปกติอะตอมหรือโมเลกุล) ในหนึ่งโมลของสารที่กำหนด ในแง่ของฆราวาสหนึ่งโมลของสารจะเป็นตัวแทนของจำนวนอะตอมและโมเลกุลที่มีอยู่ในองค์ประกอบ ตัวอย่างเช่น: ออกซิเจนมีน้ำหนักอะตอม 16 ซึ่งจะเป็นตัวแทนของมวลต่อโมลของออกซิเจน ออกซิเจนหนึ่งโมลจะมีมวล 16 กรัม จากข้อมูลของ Avogardo หนึ่งโมเลกุลของออกซิเจนจะมีจำนวนอะตอมเท่ากับไฮโดรเจนหนึ่งโมล อย่างไรก็ตามน้ำหนักอาจแตกต่างกัน
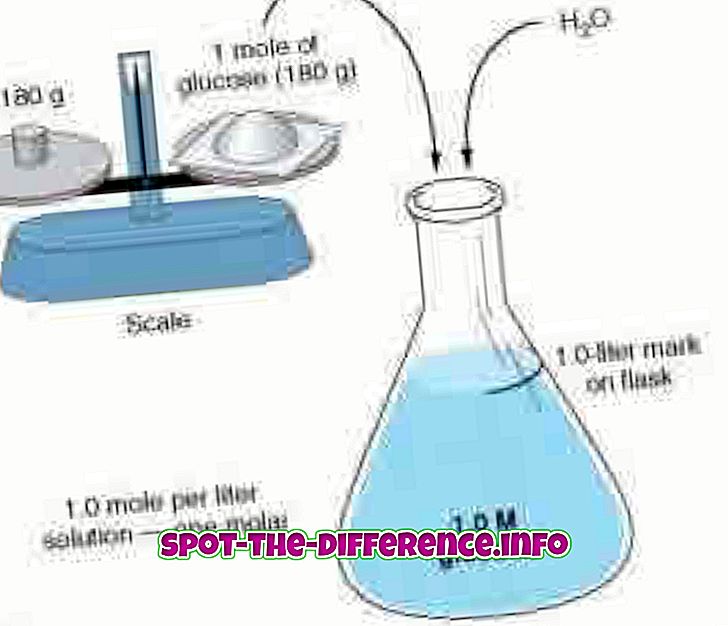
Molarity และ molality ทำการวัดความเข้มข้นโดยใช้สองวิธีที่แตกต่างกัน Molarity ยังเป็นที่รู้จักกันในนามความเข้มข้นฟันกรามวัดจำนวนโมลของสารที่มีอยู่ในลิตรต่อการแก้ปัญหา Molarity นั้นแทนด้วยเมืองหลวง M ดังนั้นวิธีแก้ปัญหาที่มี 1.0M จะระบุว่ามันมีตัวถูกละลาย 1 โมลต่อลิตรของสารละลาย ตัวอย่างเช่น: วิธีแก้ปัญหาของน้ำและน้ำตาล หากสารละลายมีค่าเป็น 1.0 M แสดงว่าสารละลายนั้นมีน้ำตาล 1 โมลต่อลิตรของสารละลาย Molarity ยังเป็นที่รู้จักกันในนามความเข้มข้นของสารปริมาณความเข้มข้นของปริมาณความเข้มข้นของสารหรือเพียงแค่ความเข้มข้น Molarity สามารถคำนวณได้โดยใช้สูตร: M = mol (# ของโมล) / L (ปริมาตรของสารละลายเป็นลิตร)

Molality ใช้วัดจำนวนโมลของสารที่มีอยู่ในตัวทำละลายต่อกิโลกรัม Molality แสดงด้วยตัวพิมพ์เล็ก m ดังนั้นวิธีแก้ปัญหาที่มี 1.0m จะระบุว่ามันมีตัวถูกละลาย 1 โมลต่อกิโลกรัมของตัวทำละลาย ลองแยกความแตกต่างจากตัวทำละลาย ตัวถูกละลายคือสารที่ถูกละลายในสารอื่น ตัวทำละลายเป็นสารที่ละลายตัวถูกละลาย ดังนั้นถ้ามีการผสมน้ำและน้ำตาลเข้าด้วยกันน้ำตาลจะเป็นตัวถูกละลายและทำให้น้ำเป็นตัวทำละลาย น้ำน้ำตาลผสมจะเป็นทางออก ตอนนี้ในโมลิมอลมันมีความสำคัญอย่างยิ่งที่โมลจะถูกหารด้วยมวลของตัวทำละลายและไม่ใช่วิธีแก้ปัญหา สามารถคำนวณ Molality ได้โดยใช้สูตร: m = mol (# ของโมล) / KG (มวลของตัวทำละลายในหน่วยกิโลกรัม)
ทำไมถึงแตกต่าง ทีนี้ทั้งคู่ถูกใช้เมื่อต้องรับมือกับอุณหภูมิ หากสารละลายมีการเปลี่ยนแปลงอุณหภูมิจะใช้โมลิลิตี้ แต่สำหรับการแก้ปัญหาที่จะยังคงอยู่ที่โมลาริตีอุณหภูมิคงที่จะใช้ นี่เป็นเพราะเมื่ออุณหภูมิเพิ่มขึ้นหรือลดลงปริมาตรของสารละลายจะเปลี่ยนแปลงและสิ่งนี้จะส่งผลโดยตรงต่อโมลาร์ ดังนั้น molality จะใช้ในการคำนวณความเข้มข้น